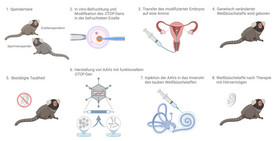
Warum sind genetisch modifizierte Tiere in der Forschung wichtig?
Säugetiere haben sich über evolutionäre Zeiträume aus gemeinsamen Vorfahren entwickelt. Daher sind die Grundbaupläne und –funktionen ihrer Organe sehr ähnlich. Sie haben zum Beispiel alle ein prinzipiell gleich aufgebautes Herz oder ein zentrales Nervensystem, das Sinneswahrnehmungen verarbeitet und Bewegungen koordiniert. Viele allgemeine Aspekte der Funktionsweise von Säugetieren, zu denen auch wir Menschen gehören, könnte man also an jeder beliebigen Säugetierart studieren und dabei Vieles über die grundlegende Funktionsweise des menschlichen Körpers lernen. Aus Arbeiten an Mäusen und Ratten, die die am häufigsten genutzten „Tiermodelle“ in der biomedizinischen Forschung sind, sind daher auch viele bahnbrechende Erkenntnisse für die Humanmedizin gewonnen worden. Ein besonderer Vorteil von Mäusen ist zusätzlich, dass es seit mehr als 30 Jahren möglich ist, ihr Erbgut gezielt zu verändern; sie transgen zu machen oder allgemein, sie genetisch zu modifizieren.
![Schematische Darstellung eines Gens innerhalb der genomischen DNA. Abbildung: Thomas Splettstoesser (www.scistyle.com), [CC BY 4.0 (http://creativecommons.org/licenses/by/4.0)], Wikimedia Commons](/fileadmin/_processed_/2/a/csm_Chromosom-DNA-Gen_032400cff2.png)
Erbkrankheiten sind genetisch bedingt
Ein wesentlicher Teil des Erbgutes (des Genoms) ist in Genen organisiert. Gene sind bestimmte Abschnitte im Genom, die die Information für eine ganz wesentliche Gruppe molekularer Bausteine (Proteine) des Körpers enthalten. Das menschliche Genom enthält etwa 23.000 unterschiedliche Gene. Schon lange kennt man Erkrankungen, die familiär gehäuft vorkommen, die also vererbt werden. Solche Erkrankungen werden als genetische Erkrankungen bezeichnet. Sie beruhen also auf einer Fehlfunktion von Genen beziehungsweise der Proteine, deren Herstellungsinformation in den entsprechenden Genen hinterlegt ist.
Zu den genetischen Erkrankungen gehören zum Beispiel Chorea Huntington oder Leukodystrophien, beides unheilbare und immer (Chorea Huntington) oder oft (Leukodystrophie) tödliche Erkrankungen. Auch so häufige und schwerwiegende Erkrankungen wie die Schüttellähmung (Parkinson’sche Erkrankung) oder Herzversagen können genetische Ursachen haben. Und seit einer Reihe von Jahren können auf Grund molekularbiologischer und technischer Innovationen die genetischen Ursachen vieler Erbkrankheiten sehr detailliert diagnostiziert werden. So weiß man inzwischen von vielen Erkrankungen, dass der Verlust der Funktion bestimmter Gene, beziehungsweise der zugehörigen Proteine, oder auch eine spezifisch veränderte Funktion eines Proteins, Krankheiten auslösen können.
Viele schwerwiegende Erkrankungen sind heute leider trotzdem immer noch unheilbar. Das liegt unter anderem daran, dass man die Ursachen einer Erkrankung beim Menschen zwar beschreiben, aber ihre Auswirkungen auf die Zellen, Organe sowie auf den ganzen Organismus nicht versteht. Das Hauptproblem dabei ist oft, dass das relevante Untersuchungsmaterial, also das erkrankte Gewebe, nicht verfügbar ist. So kann man aus ethischen und medizinischen Gründen einem Parkinsonpatienten keine Gehirngewebeprobe entnehmen, um das erkrankte Gewebe zu analysieren. Diese Tatsache verhindert ein besseres funktionelles Verständnis der Entstehung vieler Erkrankungen sowie auch die Entwicklung und Überprüfung neuer Therapieansätze. So besteht heute eine große Lücke zwischen der genetischen und molekularbiologischen Diagnostik von Erkrankungen und dem Verständnis der funktionellen Auswirkungen dieser genetischen Veränderungen im Kontext eines Gesamtorganismus beim Menschen, also des Patienten. Dieses funktionelle Verständnis ist für die Entwicklung einer Therapie aber von entscheidender Bedeutung.
Diese Lücke kann inzwischen in Teilen durch die Entwicklung und breitere Anwendung von Stammzell- und Organoidmodellen geschlossen werden. Gerade Organoide können gute Einblicke in einige Aspekte der Funktion echter Organe geben, aber auch sie sind in ihrer biologischen Komplexität und Regulation noch weit von einem in einen Gesamtorganismus eingebetteten Organ entfernt. Allerdings haben Stammzell- und Organoidmodelle den Vorteil, dass sie mit menschlichen Zellen hergestellt werden können. Wenn auch nicht auf organismischer Ebene, so spiegeln humane Stammzell- und Organoidmodelle die humane Situation auf molekularer und zellulärer Ebene besser wider als Tiermodelle. Sie sind also gemeinsam mit Tiermodellen sehr nützlich, um Krankheiten zu erforschen und Therapien zu entwickeln.
Mäuse haben sehr viele Gene, die auch im menschlichen Genom vorkommen. Trotzdem werden die entsprechenden genetischen Erkrankungen, an denen Menschen oft leiden, bei Tieren nicht immer beobachtet. (Das liegt vermutlich nicht daran, diese genetischen Erkrankungen bei Mäusen nie vorkommen, sondern daran, dass diese solchermaßen erkrankten Tiere – anders als Menschen in ärztlicher Behandlung – in der Natur einfach nicht überleben.) Oft kann dann aber das gezielte Ausschalten oder Verändern von Genen in der Maus eine Erkrankung des Menschen widerspiegeln. So ist es ein sehr hilfreicher Ansatz, die in Menschen diagnostizierten genetischen Ursachen von Erkrankungen in Mäusen nachzubilden, also transgene oder genetisch modifizierte Mäuse zu generieren und so Gewebeproben für ein besseres funktionelles Verständnis der zellbiologischen und organismischen Ursachen von Erkrankungen zu bekommen. Und um neue Therapieansätze zu testen, deren gewünschte positive Wirkungen sowie mögliche Nebenwirkungen man nicht von vornherein sicher einschätzen kann.

Warum sind genetisch veränderte Primaten wichtig?
Es gibt jedoch im menschlichen Genom auch Gene, die im Mausgenom nicht vorkommen. Diese zusätzlichen Gene, die sich erst im Verlauf der Entstehung der Primaten entwickelt haben, haben keine Entsprechung im Genom anderer Säugetiere. Sie sind primatenspezifisch, kommen also nur bei Affen und Menschen vor. Und manche Gene im Menschen, zu denen es eine grundsätzliche Entsprechung bei der Maus gibt, haben im Laufe der Evolution auch neue, zusätzliche Eigenschaften erworben. So führen neu entstandene und leicht modifizierte Gene dazu, dass wir uns als Primaten von anderen Säugetiergruppen ganz wesentlich unterscheiden, auch wenn unser Körpergrundbauplan vergleichbar ist. Niemand wird wohl abstreiten, dass wir uns von Mäusen deutlich unterscheiden. Seien es so einfach messbare Dinge wie die Pulsfrequenz, die bei uns etwa bei 60 bis 80 Schlägen pro Minute liegt, bei der Maus jedoch bei etwa 600 bis 700. Oder das Lebensalter: 70 bis 90 Jahre gegenüber ein bis zwei Jahren. Oder auch bestimmte kognitive Fähigkeiten, die wohl nur uns Menschen eigen sind. Diese Unterschiede illustrieren auch die Grenzen der Modellhaftigkeit von Mäusen, wenn es um bestimmte Erkrankungen geht, die spezifische Eigenschaften des Menschen betreffen und die andere Säugetiere nicht aufweisen.
Hier kann es Sinn machen, neben Mäusen dem Menschen evolutionär näherstehende Tiere, nämlich Affen, als Modelle zu nutzen. Affen haben ein dem Menschen vergleichbares Genom, und auch ihre Gesamtkörperfunktion ist der des Menschen ähnlicher. So ist es wahrscheinlich, dass manche Erkrankungen, die in der Maus mittels genetischer Modifikation nicht gut nachahmbar sind, im Affen auf diese Weise dargestellt werden können. Und solche genetisch modifizierten Affen könnten einen großen Schritt in Richtung eines besseren Verständnisses sehr bedeutsamer, bisher unheilbarer und tödlicher Erkrankungen bringen und damit neue Therapien in greifbarere Nähe rücken.
Dabei muss jedoch beachtet werden:
- Heute kann niemand sicher vorhersagen, ob und inwieweit genetisch modifizierte Affen tatsächlich zur Therapieentwicklung beitragen werden. Aber es ist ein rationaler und biomedizinisch gut begründeter Ansatz, der wahrscheinlich wichtige neue Erkenntnisse hinsichtlich schwerwiegender Erkrankungen des Menschen bringen wird.
- Erkenntnisgewinn und Therapieentwicklung basierend auf genetisch modifizierten Tieren allgemein, und Affen speziell, ist nur sehr langfristig zu erwarten. Realistische Zeiträume sind eher Jahrzehnte als Jahre. Angesichts der potentiellen Bedeutung transgener Primaten haben Japan, China und die USA umfangreiche Arbeiten in diesem Bereich gestartet, mit dem Ziel international führend in diesem biomedizinischen Zukunftsfeld zu werden.
- Wenn man genetisch modifizierte Tiere als Modelle für schwerwiegende und tödliche Erkrankungen des Menschen einsetzt, impliziert das auch, dass man die Tiere zu einem bestimmten Zeitpunkt einschläfert. Dieser Zeitpunkt sollte so gewählt werden, dass die Tiere nicht so leiden, wie es die Patienten teils tun, für die geforscht wird. Die Tiere sollen also nicht orientierungslos werden wie ein Alzheimerpatient oder völlig bewegungsunfähig wie ein Patient mit schwerer Verlaufsform der Parkinson’schen Erkrankung. Vielmehr ist die Nachbildung der früheren Phasen einer Erkrankung aus Forschungssicht wichtig, da man hier die entscheidenden molekular- und zellbiologischen sowie die frühen funktionellen Veränderungen untersuchen kann, die zur vollen Ausprägung einer Krankheit führen. Zudem ist es sehr viel sinnvoller, Therapieansätze in frühen Phasen zu testen, da Therapien oft ein Fortschreiten verhindern, aber ein Rückgängigmachen nicht erreichen können. Den Tieren braucht also das Leiden, das Patienten durchleben müssen, nicht zugemutet werden.
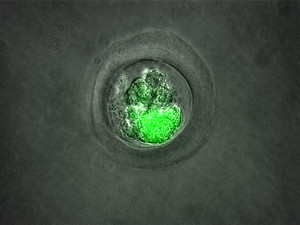
Transgene Affen am DPZ
Am DPZ wurden die Methoden für die genetische Veränderung von Weißbüschelaffen durch die Einbringung des Gens für das pathologisch inaktive Protein Green Fluorescent Protein etabliert. Aktuell erfolgen Arbeiten zur genetischen Modifikation von Weißbüschelaffen mit Hilfe des CRISP/Cas-Systems. Dieses Verfahren erlaubt die gezielte Veränderung des Erbguts von Affen und wurde an Zellkulturen auf seine Zielgenauigkeit hin überprüft. Ziel der aktuellen Arbeiten am DPZ ist es, mit Hilfe eines genetisch modifizierten, tauben Affen eine Gentherapie für genetisch bedingte Taubheit des Menschen präklinisch auf ihre Sicherheit und Wirksamkeit zu testen.
Kontakt

Prof. Dr. Rüdiger Behr Leiter Forschungsplattform Degenerative Erkrankungen +49 551 3851 132 +49 551 3851 431 Kontakt
Weitere Informationen
Informationen zu transgenen Mäusen auf "Tierversuche verstehen"
Transgene Weißbüschelaffen
Das Video zeigt eine Familie von Weißbüschelaffen in der Primatenhaltung des DPZ. Ein Teil der Tiere trägt das nicht krankmachende GFP-Transgen, das sie von der Mutter vererbt bekommen haben, ein anderer Teil weist ein unverändertes Erbgut auf. Beide, transgene und nicht-transgene Tiere, sind nicht unterscheidbar.