Coronavirus-Erkältung
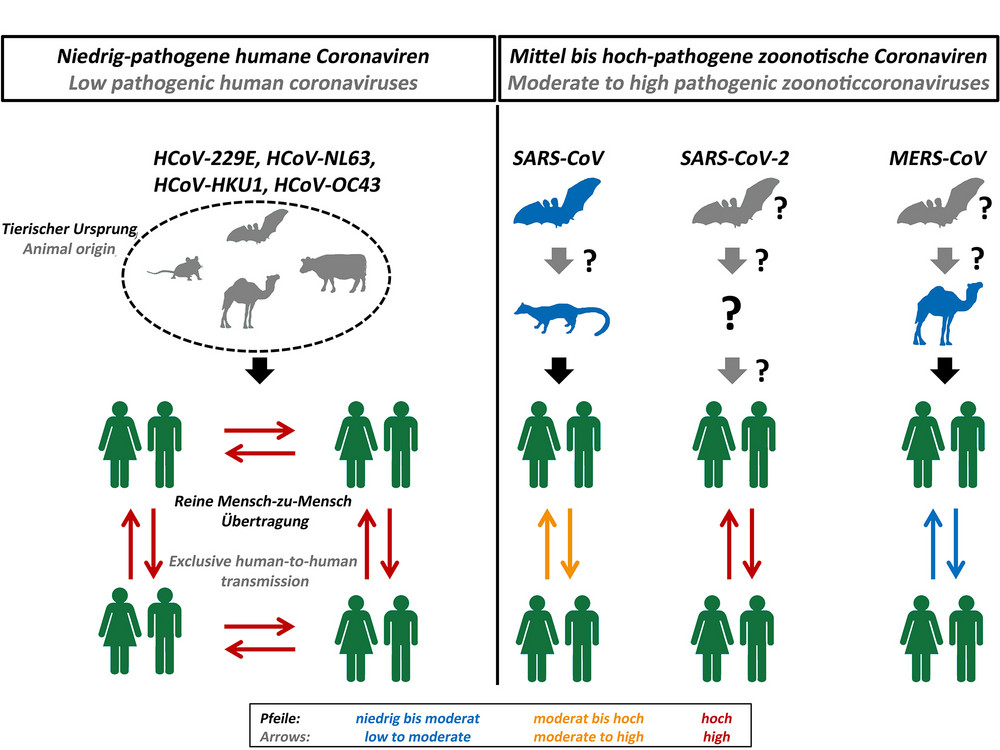
Derzeit sind vier Arten von Coronaviren bekannt, NL63, OC43, 229E und HKU1, die weltweit verbreitet sind und ganzjährig den Menschen infizieren. Eine Infektion mit diesen Viren verursacht in der Regel milde Atemwegserkrankungen. Man schätzt, dass etwa 30 Prozent aller Patienten mit Erkältungen, die beim Arzt vorstellig werden, eine Coronavirus-Infektion durchlaufen. Schwere Krankheitsverläufe sind selten und werden hauptsächlich bei Kleinkindern, älteren Menschen und immungeschwächten Patienten beobachtet. Wissenschaftliche Studien aus den letzten Jahren legen nahe, dass die Coronaviren des Menschen wahrscheinlich vor vielen Jahren von Tieren auf den Menschen übertragen wurden (Zoonose) und seitdem ständig in der Bevölkerung zirkulieren (Abbildung 1). Analog zu den Coronaviren des Menschen wurden Coronaviren auch in verschiedenen Tieren nachgewiesen (unter anderem in Igeln, Fledermäusen, Schweinen, Kamelen, Rindern und Vögeln), in denen sie teilweise schwere Erkrankungen des Verdauungstrakts und des Nervensystems hervorrufen.
Schweres-akutes Atemwegssyndrom (Severe Acute Respiratory Syndrome, SARS)
SARS ist eine schwere Lungenerkrankung
In der Wintersaison im Jahre 2002 trat im Süden Chinas eine bislang unbekannte, schwer verlaufende Lungenerkrankung auf, das severe acute respiratory syndrome (SARS). SARS breitete sich zunächst in China aus, wobei insbesondere in Krankenhäusern massive Krankheitsausbrüche beobachtet wurden. Durch Reisende wurde das Virus anschließend in zahlreiche weitere Länder verschleppt, und obwohl das Zentrum der SARS-Pandemie in Asien lag, wurden auch zahlreiche SARS-Erkrankungen zum Beispiel in Kanada beobachtet. Trotz der weltweiten Ausbreitung war die Übertragbarkeit von SARS jedoch deutlich geringer als zum Beispiel von Influenza (Grippe). Die SARS-Pandemie konnte daher durch engmaschige Kontrollen von Reisenden und Quarantänemaßnahmen im Sommer 2003 gestoppt werden, ohne dass ein Impfstoff oder ein Medikament zur Verfügung standen. Zu diesem Zeitpunkt waren knapp 800 Menschen an der Erkrankung gestorben und allein in Asien war ein wirtschaftlicher Schaden von etwa 30 bis 50 Milliarden US-Dollar entstanden. Nach dem großen SARS-Ausbruch von 2002/2003 wurden noch im Winter 2004 vereinzelte, mild verlaufende SARS-Infektionen beobachtet. Außerdem kam es zu einer Laborinfektion und zu einer nachfolgenden Übertragung des Virus auf Kontaktpersonen. Seither wurden keine weiteren SARS-Infektionen beschrieben.
Der SARS-Erreger ist ein Coronavirus
Zu Beginn der SARS-Pandemie war noch unklar, welcher Erreger hinter der Erkrankung steckt. Es wurde jedoch bereits nach kurzer Zeit mittels der Polymerase-Kettenreaktion und Elektronenmikroskopie ein neues Coronavirus in SARS-Patienten nachgewiesen. Anschließend konnte gezeigt werden, dass das Virus die sogenannten Koch`schen Postulate erfüllt: Es war immer in SARS-Patienten nachweisbar, konnte in Zellkulturen vermehrt werden und löste in infizierten Tieren eine SARS-ähnliche Erkrankung aus. Außerdem konnte das Virus aus infizierten Tieren isoliert werden. Damit war klar, dass das neue Coronavirus für SARS verantwortlich ist. Dementsprechend wurde dieses Virus fortan SARS-Coronavirus genannt.
Das SARS-Coronavirus wird von Tieren auf den Menschen übertragen
Im Zuge der Aufarbeitung des SARS-Ausbruchs und der Suche nach seinem Ursprung wurden dem SARS-Coronavirus sehr ähnliche Viren in Fledermäusen nachgewiesen. Es wurde daher die Schlussfolgerung gezogen, dass Fledermäuse das sogenannte natürliche Reservoir des SARS-Coronavirus darstellen. Allerdings scheinen diese Fledermäuse das Virus nicht direkt auf den Menschen übertragen zu haben. Dafür waren Zwischenwirte verantwortlich – die Zibetkatze sowie der Marderhund (Abbildung 1). Diese Tiere werden in bestimmten Regionen Chinas vor allem in Restaurants zum Verzehr angeboten und auf Märkten gehandelt. Es gilt mittlerweile als gesichert, dass die ersten SARS-Coronavirus-Infektionen auf den Besuch eines Marktes auf dem (Wild-)Tiere zum Verkauf angeboten wurden (sogenannte wet markets) zurückzuführen sind.
Das zelluläre Protein ACE2 spielt eine wichtige Rolle in der SARS-Coronavirus-Infektion
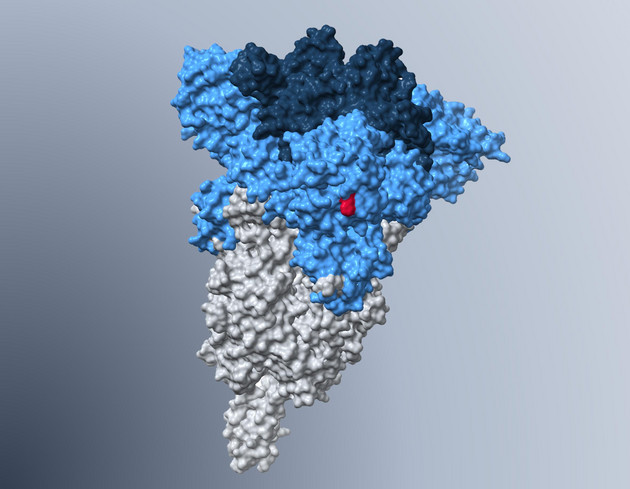
Coronaviren verwenden eines ihrer Hüllproteine, das Spike (S) Protein, um in Wirtzellen einzudringen. Dazu muss das S-Protein an einen geeigneten Rezeptor auf der Oberfläche von Zellen binden. Das SARS-Coronavirus verwendet hierfür das zelluläre Protein angiotensin converting enzyme 2 (ACE2) (Abbildung 2). Dabei scheint die Interkation zwischen dem S-Protein und ACE2 die Übertragbarkeit des Virus und die Fähigkeit SARS auszulösen, wesentlich zu bestimmen. Es wurden nur solche Varianten des SARS-Coronavirus zwischen Menschen übertragen beziehungsweise in Patienten nachgewiesen, die hocheffizient an ACE2 binden konnten. Dabei ist bemerkenswert, dass ACE2 nicht nur für den Viruseintritt in Zellen wichtig ist, sondern möglicherweise auch eine Rolle bei der Ausbildung der SARS-Erkrankung spielt. Das ACE2-Protein hat normalerweise die Aufgabe, die Lungen vor Schädigung zu schützen und diese wichtige Funktion von ACE2 wird durch die Infektion mit dem SARS-Coronavirus verringert.
Mittlerer-Osten Atemwegssyndrom (Middle East Respiratory Syndrome, MERS)
Das Middle East Respiratory Syndrome (MERS) wurde erstmals im Jahr 2012 in Saudi-Arabien beobachtet. MERS ist eine schwere Lungenerkrankung, die Ähnlichkeiten zu SARS aufweist und durch das MERS-Coronavirus ausgelöst wird. Im Vergleich zu einer Infektionen mit dem SARS-Coronavirus ist die MERS-Coronavirus-Infektion mit einer deutlich höheren Sterblichkeitsrate verbunden: Während etwa zehn Prozent der SARS-Coronavirus infizierten Patienten versterben, ist bei ungefähr 30 Prozent der MERS-Coronavirus-Infektionen ein tödlicher Verlauf zu beobachten. Dabei weisen MERS-Patienten mit Vorerkrankungen - wie beispielsweise Diabetes - ein erhöhtes Risiko auf, einen tödlichen Verlauf zu entwickeln. Analog zur SARS-Epidemie wurden massive MERS-Ausbrüche in Krankenhäusern beobachtet und das Virus wurde durch infizierte Reisende in zahlreiche Länder eingeschleppt. So konnte ein großer MERS-Ausbruch in Südkorea mit mehr als 100 Infektionen auf einen infizierten Reisenden zurückgeführt werden.
Das MERS-Coronavirus wird von Dromedaren (einhöckrigen Kamelen) auf den Menschen übertragen (Abbildung 1). Eine nachfolgende Mensch-zu-Mensch Übertragung ist gegenwärtig selten, da diese glücklicherweise nicht sehr effizient ist. Allerdings wird befürchtet, dass das Virus Mutationen erwerben könnte, die die Übertragbarkeit zwischen Menschen erhöhen. Dabei könnte es sich um Mutationen handeln, welche die Virus-Vermehrung in den oberen Atemwegen (Nasen- und Rachenraum) verstärken: Man geht davon aus, dass die ausgeprägte Fähigkeit des MERS-Coronavirus sich in den unteren Atemwegen (Lunge) zu vermehren, für die Schwere der ausgelösten MERS-Erkrankung verantwortlich ist. Im Gegensatz dazu vermehrt sich das Virus in den oberen Atemwegen nur schwach und dies erklärt, warum das Virus derzeit nur ineffizient zwischen Menschen übertragen wird. Ein ähnlicher Zusammenhang wird für das SARS-Coronavirus vermutet. Es ist herauszustellen, dass MERS-Coronavirus-Infektionen im Mittleren Osten auch heute noch beobachtet werden und die Gefahr einer weltweiten Verbreitung nach wie vor besteht.
Forschung zum SARS-Coronavirus-2 am DPZ
Die Abteilung Infektionsbiologie erforscht, wie Coronaviren in Zellen eindringen. Im Fokus der Forschung steht dabei das virale Spike-Protein (S). Das Spike-Protein auf der Virusoberfläche dient dem Virus als Schlüssel zur Wirtszelle. Es erlaubt dem Virus, sich an Zellen anzuheften und anschließend mit den Zellen zu verschmelzen. So schleust es seine Erbinformation für die virale Vermehrung in die Zellen ein.
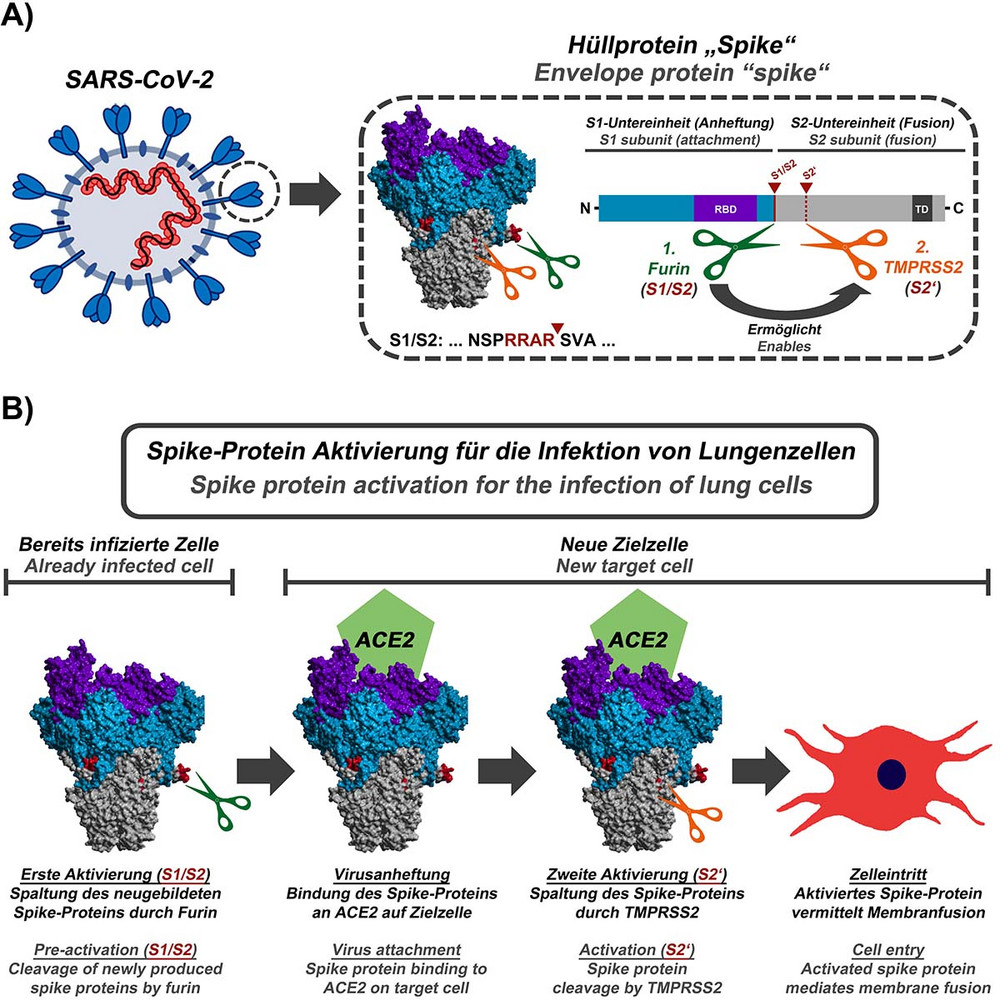
Dazu müssen Aktivierungssequenzen des Spike-Proteins durch Enzyme der Zellen, sogenannte Proteasen, gespalten werden. Das Spike-Protein von SARS-CoV-2 trägt eine Aktivierungssequenz an der sogenannten S1/S2-Spaltstelle, die man von hochpathogenen Vogelgrippe-Viren kennt, aber in SARS-CoV-2 eng verwandten Viren bislang nicht finden konnte. Die Bedeutung dieser Sequenz für das Virus war bisher unbekannt.
Die Infektionsbiologen des Deutschen Primatenzentrums um Markus Hoffmann und Stefan Pöhlmann konnten in einer Studie (veröffentlicht am 1. Mai 2020) zeigen, dass die S1/S2-Aktivierungssequenz des Spike-Proteins von SARS-CoV-2 durch die zelluläre Protease Furin gespalten wird. Diese Spaltung ist für die Infektion von Lungenzellen unverzichtbar. Außerdem ist sie für die Verschmelzung von infizierten Zellen mit nicht-infizierten Zellen wichtig, ein weiterer Weg, wie sich das Virus im Körper ausbreiten könnte, ohne die Wirtszelle zu verlassen.
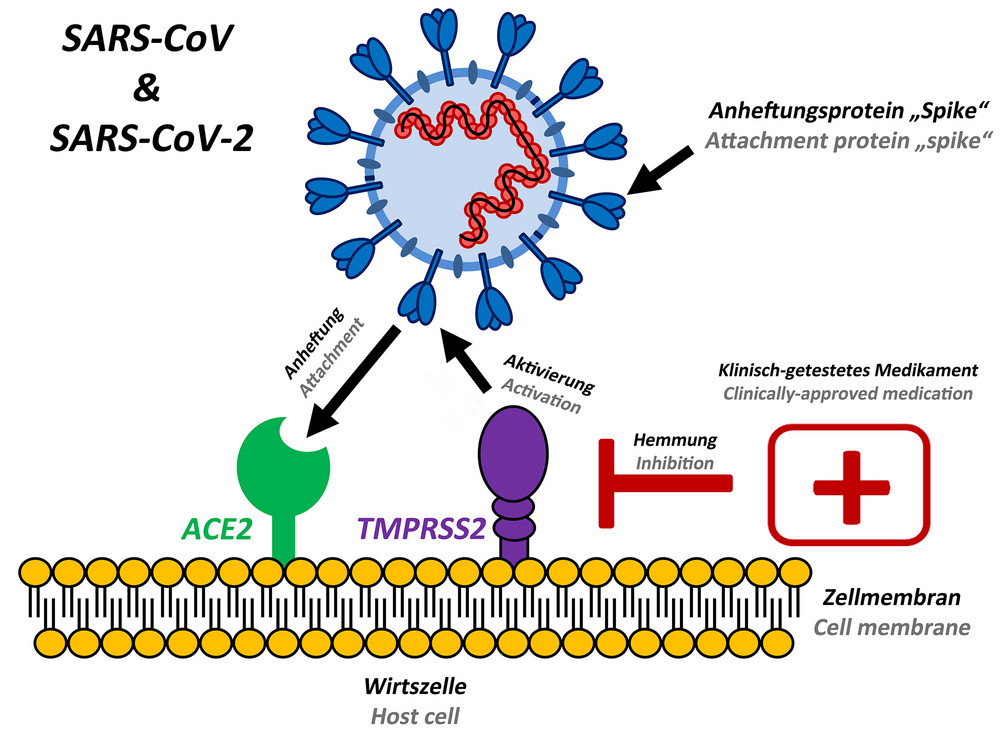
In einer zuvor erschienen Studie zu SARS-CoV-2 (publiziert am 5. März 2020) konnten die Infektionsbiologen zeigen, dass das Spike-Protein des SARS-Coronavirus 2 neben dem zellulären Protein ACE2 auch die zelluläre Serinprotease TMPRSS2 für den Zelleintritt benötigt (Abbildung 2). Außerdem konnte demonstriert werden, dass ein Medikament, Camostat, das TMPRSS2 hemmt und für den Einsatz im Menschen in Japan freigegeben wurde, die SARS-CoV-2-Infektion von Lungenzellen blockiert (Abbildung 2). Es ist daher möglich, dass dieses Medikament die Ausbildung von COVID-19 verhindern kann. Diese Ergebnisse wurden in der renommierten Fachzeitschrift Cell publiziert.
Im Rahmen des vom Bund geförderten Projekts "RENACO" (repurposing nafamostat mesylate for COVID-19 prevention) in Kooperation mit dem Fraunhofer ITEM in Hannover wird das Bauchspeicheldrüsen-Medikament Nafamostat, das eine 50-fach hörere antivirale Wirksamkeit als Camostat aufweist, im Hinblick auf eine mögliche Wirksamkeit gegen SARS-CoV-2 getestet. Ziel ist die Entwicklung von Nafamostat als Medikament in Form eines Sprays zur direkten Applikation in die oberen Lungenwege für die Behandlung von COVID-19. Erste Ergebnisse zeigen, dass Camostat und Nafamostat die Vermehrung von SARS-CoV-2 in Lungengewebe in Zellkultur hemmen. Zudem konnte im Rahmen der Studie gezeigt werden, dass auch das Camostat-Abbauprodukt GBPA, dass im Körper aus Camostat gebildet wird, antiviral wirksam ist und dass SARS-CoV-2 in der Lage ist, auch verwandte TMPRSS2-verwandte Enzyme in den oberen Atemwegen für den Eintritt in die Wirtszellen zu nutzen.
In einer weiteren Studien konnten die Forschenden in Kooperation mit der Charité in Berlin und der Rheinischen Friedrich-Wilhelms-Universität Bonn bereits zeigen, dass das Malaria-Medikament Chloroquin eine SARS-CoV-2-Infektion von Lungenzellen in Zellkultur nicht blockieren kann und somit nicht für eine Behandlung von COVID-19 eingesetzt werden sollte. SARS-CoV-2 ist in der Lage, entweder durch Anlagerung an die Zellen direkt mit der Membran zu verschmelzen und sein Erbgut in die Wirtszelle einzuschleusen oder durch Einstülpung der Wirtszellmembran und Abschnürung von Transportstrukturen, sogenannte Endosomen, ins Innere der Zellen zu gelangen. In beiden Fällen wird die Anheftung des Virus an die Zellen und der nachfolgende Eintritt durch das Spike-Protein des Virus vermittelt, das entweder durch das Enzym Cathepsin L (in Endosomen) oder durch das Enzym TMPRSS2 (an der Zelloberfläche) aktiviert werden muss. Je nach Zelltyp können beide Enzyme oder nur eines von ihnen zur Aktivierung zur Verfügung stehen. Da Chloroquin die Infektion von Affen-Nierenzellen mit SARS-CoV-2 hemmt, wurde dieses Malaria-Medikament als möglicher Kandidat für die Behandlung von COVID-19 in klinischen Studien getestet. Die Studie zeigt, dass Chloroquin den Virus-Eintritt in diese Zellen verhindert, wahrscheinlich durch die Hemmung von Cathepsin L. Dies warf die Frage auf, ob Chloroquin auch die Infektion von Lungenzellen hemmt, von denen bekannt ist, dass sie zwar TMPRSS2, aber nur wenig Cathepsin L produzieren. Es konnte gezeigt werden, dass Chloroquin den SARS-CoV-2-Eintritt in menschliche Lungenzellen und die nachfolgende Ausbreitung des Virus in diesen Zellen nicht verhindert.
Im Weiteren haben die Infektionsbiologen in Zellkultur Hinweise darauf gefunden, dass Antikörper von genesenen oder geimpften Personen mutierte Viren schlechter hemmen. In Kooperation mit dem Universitätsklinikum Ulm wurde einerseits herausgefunden, dass die SARS-CoV-2 Varianten B.1.351 (Südafrika) und P.1 (Brasilien) weniger wirksam durch einen Antikörper gehemmt werden, der für die COVID-19-Therapie eingesetzt wird. Außerdem werden die Varianten weniger effektiv durch Antikörper von genesenen Patienten sowie von geimpften Personen gehemmt. Eine durchgemachte Erkrankung sowie eine Impfung könnten daher gegen diese Virus-Mutanten nur unvollständig schützen.
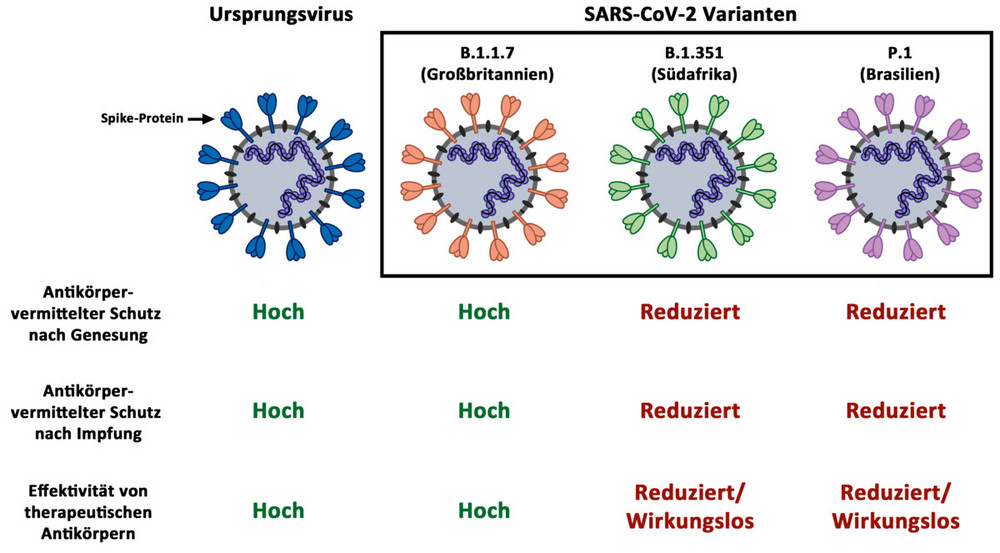
Gleiches gilt für SARS-CoV-2-Varianten, die in Nerzen entstanden sind. Bei den Nerz-Varianten wies das Spike-Protein unter anderem die Y453F-Mutation auf, die die wirksame Hemmung eines für die COVID-19-Therapie eingesetzten Antikörpers reduzierte. Zudem verminderte diese Mutation die Hemmung des Virus durch Antikörper, die nach einer durchgemachten SARS-CoV-2-Infektion gebildet wurden.
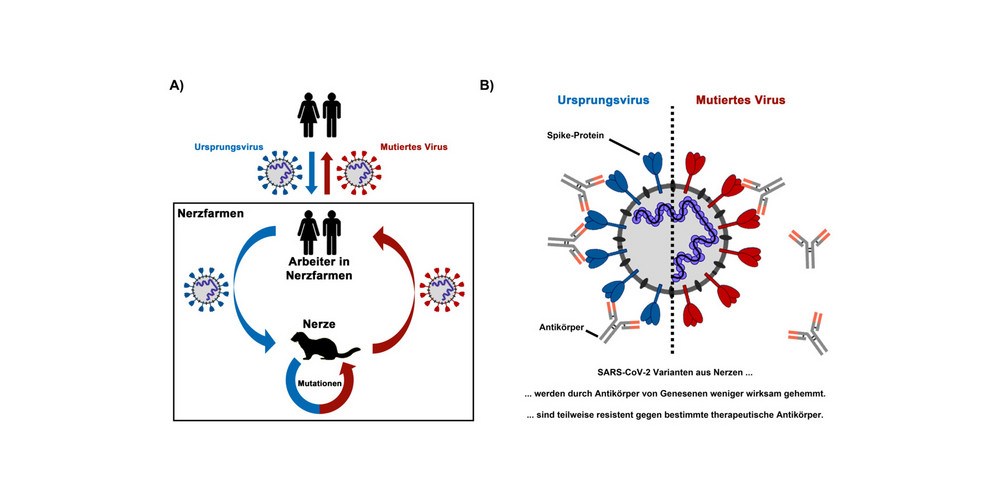
In einem weiteren Forschungsprojekt kooperiert die Abteilung Primatengenetik am DPZ mit der Universität Düsseldorf. Es ist bekannt, dass eine Infektion mit Zytomegalie-Viren (CMV) bei einem Drittel der befallenen Menschen bewirkt, dass der Körper langlebige, adaptive Natürliche Killerzellen (NK-Zellen) bildet. Diese NK-Zellen können schneller auf ein Wiederaufflammen der im Körper schlummernden CMV-Viren reagieren. Die Forschenden möchten herausfinden, ob die durch die CMV-Infektion hervorgerufenen adaptiven NK-Zellen eine positive oder negative Rolle im Krankheitsverlauf bei COVID-19 haben. Dazu werden adaptive NK-Zellen aus Blutproben von SARS-CoV-2 Patienten mit mildem beziehungsweise mit schwerem Krankheitsverlauf gewonnen und funktionell untersucht. Parallel dazu werden adaptive NK-Zellen aus Blutproben von Rhesusaffen analysiert. Die Ergebnisse sollen dazu dienen, einerseits mehr über adaptive NK-Zellen zu lernen und andererseits auch eine Methode zu erhalten, mit der man relativ leicht eine Prognose für den Krankheitsverlauf bei COVID-19 in CMV-positiven Patient*innen erstellen kann.
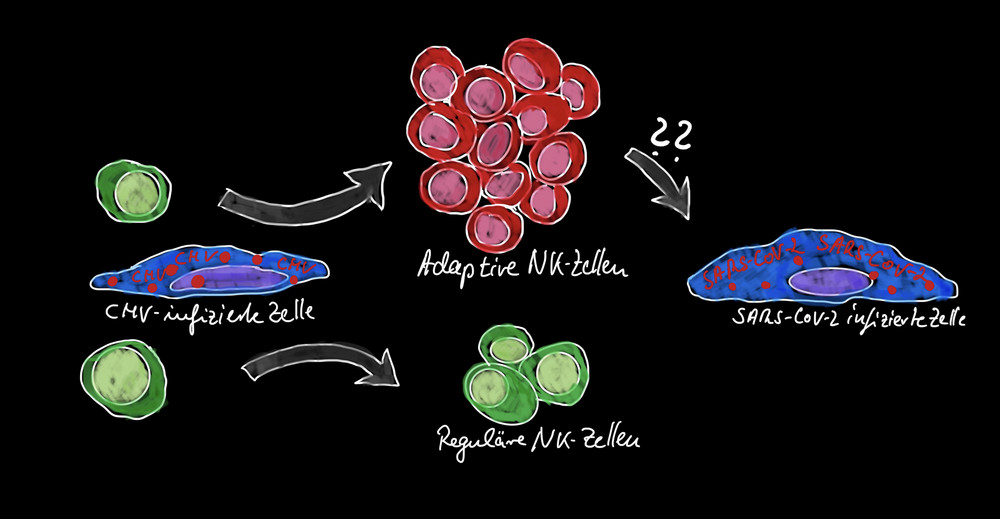
Im Weiteren haben die Forschenden der Abteilung Infektionsbiologie die Virus-Variante B.1.617 sowie die daraus hervorgegangenen Variante Delta (B.1.617.2) und deren Subtyp Delta Plus genauer untersucht. In Zellkulturstudien fanden sie heraus, dass schon die Ausgangsvariante B.1.617 bestimmte Lungen- und Darmzelllinien besser infizieren kann als das Ursprungsvirus. Außerdem konnten die Forschenden nachweisen, dass B.1.617 von Antikörpern aus dem Blut von genesenen oder geimpften Personen sowie durch einen therapeutischen Antikörper weniger gut gehemmt wird. Die B.1.617-Variante trägt acht verschiedene Mutationen im Spike-Protein, darunter zwei innerhalb der Rezeptorbindedomäne, die für die Anheftung von Viren an Zellen essentiell ist und das Hauptziel von neutralisierenden Antikörpern darstellt.
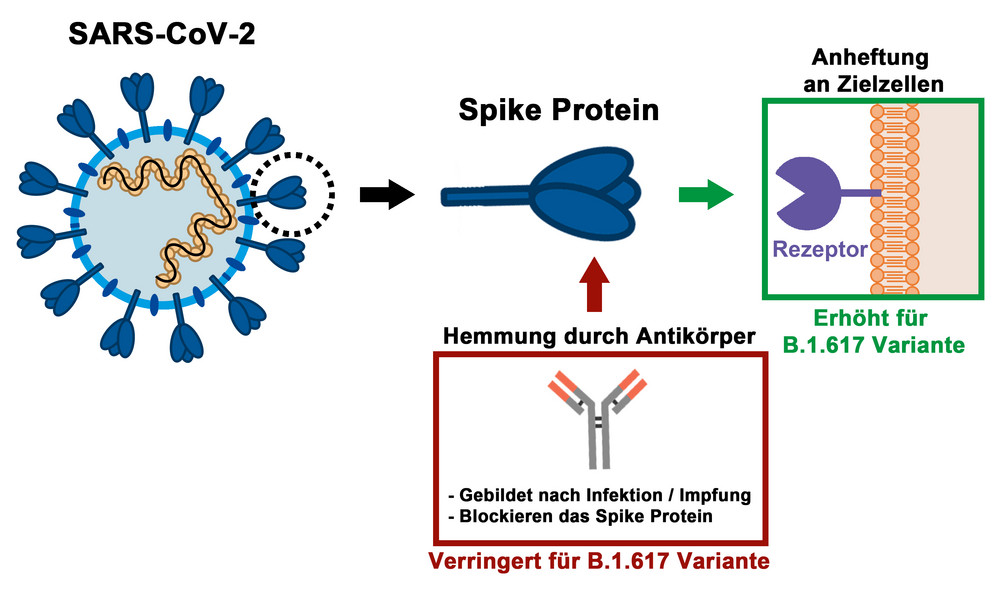
Die Delta-Variante (B.1.617.2) hat sich von Indien aus in kurzer Zeit weltweit ausgebreitet. Außerdem wurden sogenannte Delta-Plus-Viren beobachtet, die zusätzliche Mutationen tragen, die sie möglicherweise gefährlicher machen. In Zusammenarbeit mit Forschenden der Medizinischen Hochschule Hannover, der Universitätsmedizin Göttingen und der Friedrich-Alexander-Universität Erlangen-Nürnberg haben die DPZ-Infektionsbiologen untersucht, warum sich die Delta-Variante so schnell ausbreitet und ob Delta-Plus-Viren besonders gefährlich sind. In Zellkulturstudien konnten sie zeigen, dass Delta und Delta Plus Lungenzellen besser infizieren als das Ursprungsvirus. Zudem war einer von vier zur Behandlung von COVID-19 eingesetzten Antikörpern gegen Delta nicht wirksam und Delta Plus war sogar gegen zwei der Antikörper resistent. Auch Antikörper, die nach Impfung mit den Vakzinen von BioNtech-Pfizer und Oxford-AstraZeneca gebildet wurden, waren gegen Delta und Delta Plus weniger wirksam als gegen das Ursprungsvirus. Delta und Delta Plus wurden dagegen vergleichbar gehemmt, weswegen man davon ausgehen kann, dass Delta Plus für Geimpfte wahrscheinlich keine größere Gefahr darstellt als Delta. Schließlich hatten Personen, die zuerst mit Oxford-AstraZeneca und dann mit BioNtech-Pfizer geimpft wurden, deutlich mehr Antikörper, die Delta hemmten, als Personen, die zweimal mit Oxfod-AstraZeneca geimpft wurden. Die Kombination von Impfstoffen könnte daher geeignet sein, um einen besonders starken Schutz gegen SARS-CoV-2-Varianten aufzubauen.
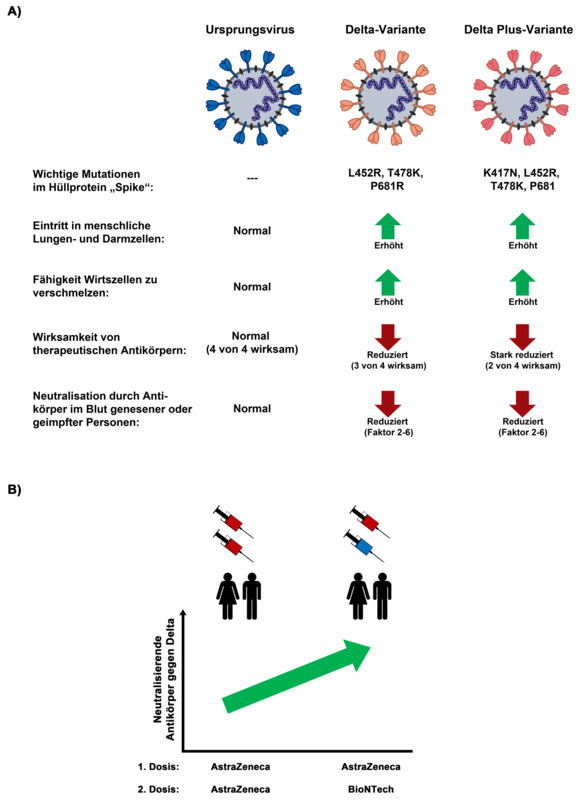
A) Zusammenfassung besonderer Eigenschaften der SARS-CoV-2 Delta- und Delta-Plus-Varianten im Vergleich zum Ursprungsvirus.
B) Eine Kreuzimpfung mit dem Vektorimpfstoff von Oxford-AstraZeneca und dem mRNA-Impfstoff von BioNTech-Pfizer führt zur Bildung von deutlich mehr neutralisierenden Antikörpern gegen die Delta-Variante als eine Doppelimpfung mit Oxford-AstraZeneca. Abbildung: Markus Hoffmann
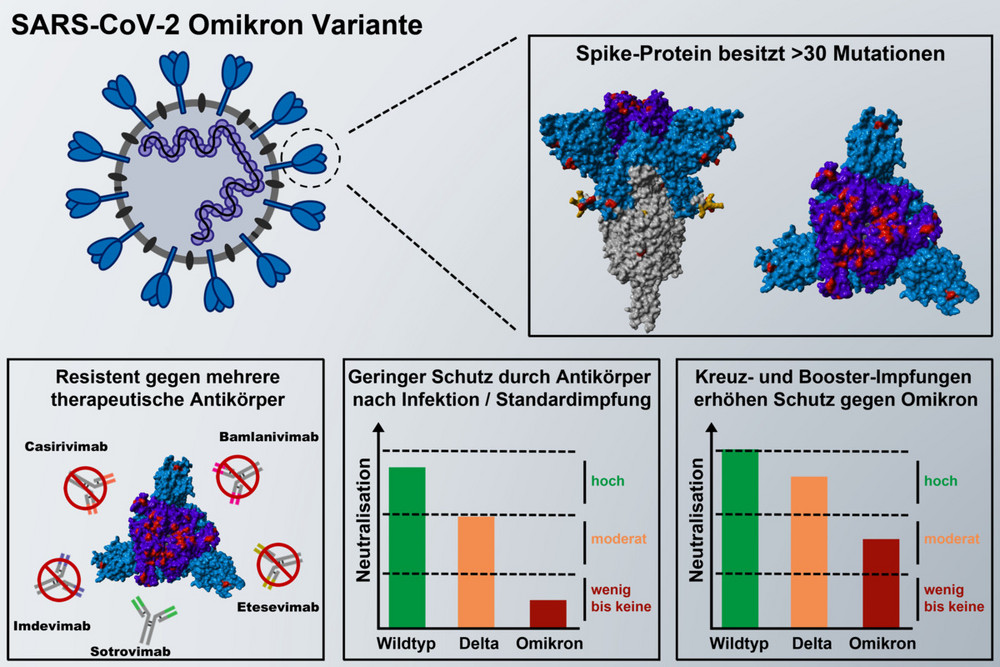
Zellkulturstudien zur Resistenz der Omikron-Variante gegen Antikörper
Die in Südafrika entdeckte Omikron-Variante (B.1.1.529) verbreitet sich und löst die Delta-Variante ab. Ein Forschungsteam um Stefan Pöhlmann und Markus Hoffmann vom Deutschen Primatenzentrum – Leibniz-Institut für Primatenforschung in Göttingen sowie Forschenden an der Medizinischen Hochschule Hannover, der Universitätsmedizin Göttingen, der Friedrich-Alexander Universität Erlangen-Nürnberg sowie des Deutschen Zentrum für Infektionsforschung in Braunschweig hat in Zellkuturen untersucht, wie effizient die Omikron-Variante durch Antikörper von Genesenen und Geimpften neutralisiert wird. Das Team konnte zeigen, dass Antikörper von Genesenen die Omikron-Variante kaum hemmen. Auch die nach zweifacher BioNTech-Pfizer Impfung gebildeten Antikörper wiesen gegen die Omikron-Variante eine deutlich geringere Wirksamkeit als gegen die Delta-Variante auf. Eine bessere Hemmung wurde nach dreifacher BioNTech-Pfizer-Impfung ebenso wie nach Kreuzimpfung mit Oxford-AstraZeneca und BioNTech-Pfizer beobachtet. Außerdem konnte das Team zeigen, dass die meisten der in der Studie untersuchten therapeutischen Antikörper, die für die Behandlung von COVID-19 eingesetzt werden, nicht gegen die Omikron-Variante wirksam sind. Die Ergebnisse deuten jedoch auch darauf hin, dass eine dritte Immunisierung mit dem BioNTech-Pfizer Impfstoff (Booster) sowie eine Kreuzimmunisierung mit Oxford-AstraZeneca und BioNTech-Pfizer gut gegen die Omikron-Variante schützen könnten. (Eine Hemmung durch T-Zellen wurde in dieser Studie nicht untersucht.)
Abteilung Infektionsbiologie
Neuigkeiten
Aktuelle Publikationen
Hoffmann, M., Krüger, N., Schulz, S., Cossmann, A., Rocha, C., Kempf, A., Nehlmeier, I., Graichen, L., Moldenhauer, A.-S., Winkler, M.S., Lier, M., Dopfer-Jablonka, A., Jäck, H.-M., Behrens, G.M.N., Pöhlmann, S., The Omicron variant is highly resistant against antibody-mediated neutralization – implications for control of the COVID-19 pandemic, Cell (2022), doi: doi.org/10.1016/j.cell.2021.12.032.
Behrens GM, Cossmann A, Stankov MV, Nehlmeier I, Kempf A, Hoffmann M, Pöhlmann S. SARS-CoV-2 delta variant neutralisation after heterologous ChAdOx1-S/BNT162b2 vaccination. The Lancet. 2021 Sep 18;398(10305):1041-1042. doi: 10.1016/S0140-6736(21)01891-2
Arora P, Sidarovich A, Krüger N, Kempf A, Nehlmeier I, Graichen L, Moldenhauer AS, Winkler MS, Schulz S, Jäck HM, Stankov MV, Behrens GMN, Pöhlmann S, Hoffmann M. B.1.617.2 enters and fuses lung cells with increased efficiency and evades antibodies induced by infection and vaccination, Cell Reports, 2021, 109825, ISSN 2211-1247, https://doi.org/10.1016/j.celrep.2021.109825
Arora P, Kempf A, Nehlmeier I, Graichen L, Sidarovich A, Winkler MS, Schulz S, Jäck HM, Stankov MV, Behrens GMN, Pöhlmann S, Hoffmann M. Delta variant (B.1.617.2) sublineages do not show increased neutralization resistance. Cell Mol Immunol. 2021; https://doi.org/10.1038/s41423-021-00772-y
Hoffmann M, Hofmann-Winkler H, Krüger N, Kempf A, Nehlmeier I, Graichen L, Arora P, Sidarovich A, Moldenhauer A-S, Winkler MS, Schulz S, Jäck H-M, Stankov MV, Behrens GMN, Pöhlmann S (2021): SARS-CoV-2 variant B.1.617 is resistant to Bamlanivimab and evades antibodies induced by infection and vaccination. Cell Reports. DOI: https://doi.org/10.1016/j.celrep.2021.109415
In den Medien
Stefan Pöhlmann im Interview im Ärztenachrichtendienst (nur für Abonnenten)
https://www.aend.de/article/216320
Links zu nationalen Seiten
Links zu internationalen Seiten
Wie Sars-CoV-2 in Zellen eindringt
Die Animation zeigt, wie Sars-CoV-2 in Zellen eindringt und wie ein Medikament (Camostat Mesilate) den Zelleintritt verhindern könnte. Animation: www.visu-l.tv