Delta und Delta Plus weichen der Antikörperantwort aus
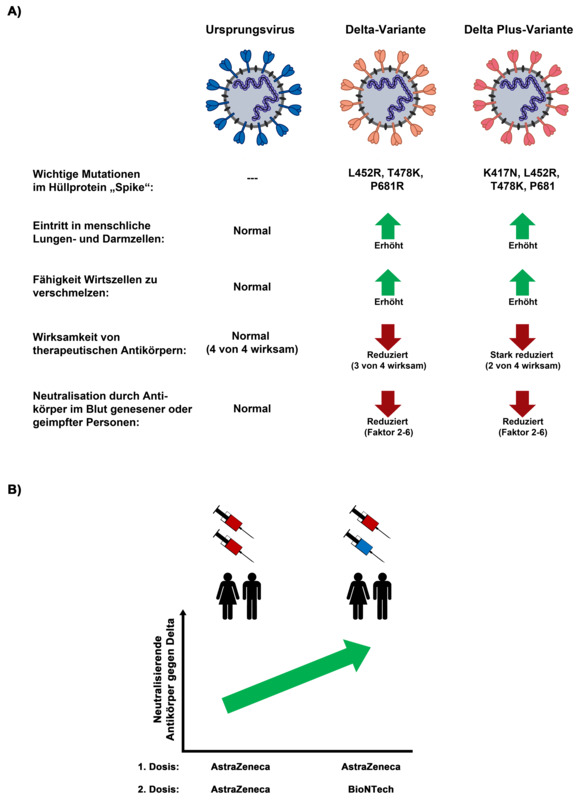

Das Auftreten von neuen SARS-CoV-2-Varianten, die sich schnell ausbreiten und den Impfschutz unterlaufen können, gefährdet das Ende der COVID-19-Pandemie. Die Delta-Variante (B.1.617.2) hat sich von Indien aus in kurzer Zeit weltweit ausgebreitet und auch in Deutschland gehen fast alle Infektionen auf diese Variante zurück. Außerdem wurden sogenannte Delta Plus Viren beobachtet, die zusätzliche Mutationen tragen, die sie möglicherweise gefährlicher machen. Ein Forschungsteam um Stefan Pöhlmann und Markus Hoffmann vom Deutschen Primatenzentrum (DPZ) – Leibniz-Institut für Primatenforschung in Göttingen sowie Forschende an der Medizinischen Hochschule Hannover, der Universitätsmedizin Göttingen und der Friedrich-Alexander-Universität Erlangen-Nürnberg haben untersucht, warum sich die Delta-Variante so schnell ausbreitet, und ob Delta Plus Viren besonders gefährlich sind. Sie konnten zeigen, dass Delta und Delta Plus Lungenzellen besser infizieren als das Ursprungsvirus. Zudem war einer von vier zur Behandlung von COVID-19 eingesetzten Antikörpern gegen Delta nicht wirksam und Delta Plus war sogar gegen zwei der Antikörper resistent. Auch Antikörper, die nach Impfung mit den Vakzinen von BioNTech-Pfizer und Oxford-AstraZeneca gebildet wurden, waren gegen Delta und Delta Plus weniger wirksam als gegen das Ursprungsvirus. Delta und Delta Plus wurden dagegen vergleichbar gehemmt, weswegen man davon ausgehen kann, dass Delta Plus für Geimpfte wahrscheinlich keine größere Gefahr darstellt als Delta. Schließlich hatten Personen, die zuerst mit Oxford-AstraZeneca und dann mit BioNTech-Pfizer geimpft wurden, deutlich mehr Antikörper, die Delta hemmten, als Personen, die zweimal mit Oxford-AstraZeneca geimpft wurden. Die Kombination von Impfstoffen könnte daher geeignet sein, um einen besonders starken Schutz gegen SARS-CoV-2-Varianten aufzubauen. (The Lancet, Cell Reports, Cell Mol Immunol)
Mehr als 99 Prozent der SARS-Coronavirus-2 Infektionen in Deutschland gehen laut Robert Koch Institut derzeit auf die Delta-Variante zurück. Mit Hilfe von Experimenten in Zellkultur konnte das Team um Stefan Pöhlmann und Markus Hoffmann zeigen, dass Delta im Vergleich zum Ursprungsvirus (das Virus, das sich in der führen Phase der Pandemie ausgebreitet hat) besser in Lungenzellen eindringen kann. Zudem gelingt es Delta besser, infizierte Lungenzellen mit nicht infizierten Zellen zu verschmelzen. „Es ist denkbar, dass sich die Delta-Variante durch die Verschmelzung von Zellen in den Atemwegen besser ausbreiten und größeren Schaden anrichten kann. Das könnte zu schwereren COVID-19-Verläufen beitragen“, vermutet Prerna Arora, Wissenschaftlerin am Deutschen Primatenzentrum und Erstautorin zweier Studien, die sich speziell mit der Delta- und Delta Plus-Variante befassen.
Zur Behandlung von COVID-19 werden monoklonale Antikörper eingesetzt. Monoklonale Antikörper sind Proteine, die gentechnisch hergestellt werden. Anders als unser Immunsystem, das bei einer Infektion eine Vielzahl von Antikörpern gegen den Erreger produziert, werden also für die COVID-19-Therapie nur isolierte Antikörper oder Kombinationen dieser Antikörper eingesetzt. Vier dieser Antikörper hat das Team um Stefan Pöhlmann und Markus Hoffmann untersucht. Dabei zeigte sich, dass Delta resistent ist gegen den Antikörper Bamlanivimab. Delta Plus ist resistent gegen zwei Antikörper: Bamlanivimab und Etesevimab, die bei der Behandlung von Erkrankten in Kombination eingesetzt werden.
Dass Delta und Delta Plus weniger gut durch Antikörper von infizierten und geimpften Personen gehemmt (neutralisiert) werden als das Ursprungsvirus, hat wahrscheinlich zur raschen Ausbreitung von Delta beigetragen. Ein Vergleich von Delta und Delta Plus zeigte, dass beide Viren vergleichbar neutralisiert werden. „Das bedeutet, dass die Impfung wahrscheinlich einen vergleichbaren Schutz gegen Delta und Delta Plus vermittelt und Delta Plus nicht deutlich gefährlicher ist", sagt Stefan Pöhlmann. Der Impfstoff von BioNTech-Pfizer wird in Europa am häufigsten eingesetzt, gefolgt vom Impfstoff von Oxford-AstraZeneca. Aufgrund von sehr seltenen Nebenwirkungen nach Impfung mit Oxford-AstraZeneca wird in Deutschland und anderen Ländern empfohlen, dass bei Personen, die bereits eine erste Impfung mit Oxford-AstraZeneca erhalten haben, BioNTech-Pfizer für die zweite Impfung eingesetzt wird. Man spricht von einer Kreuzimpfung. „Unsere Studien zeigen, dass die Kreuzimpfung deutlich mehr neutralisierende Antikörper gegen Delta induziert als zwei Impfungen mit Oxford-AstraZeneca. Personen, die eine solche Kreuzimpfungen erhalten haben, könnte daher besonders gut vor Delta und Delta Plus geschützt sein", sagt Markus Hoffmann.
„Unsere Ergebnisse decken sich mit der Beobachtung, dass Impfungen effizient vor einer schweren Erkrankung nach Infektion mit Delta schützen, aber die Infektion häufig nicht vollständig unterdrücken können. In Anbetracht des starken Schutzes vor schwerer Erkrankung muss das Ziel weiterhin eine möglichst hohe Impfquote sein. Dies sollte verhindern, dass bei einer starken Ausbreitung von Delta und eng verwandten Viren in den Wintermonaten das Gesundheitssystem überlastet wird“, sagt Stefan Pöhlmann.
Originalpublikationen
Behrens GM, Cossmann A, Stankov MV, Nehlmeier I, Kempf A, Hoffmann M, Pöhlmann S. SARS-CoV-2 delta variant neutralisation after heterologous ChAdOx1-S/BNT162b2 vaccination. The Lancet. 2021 Sep 18;398(10305):1041-1042. doi: 10.1016/S0140-6736(21)01891-2
Arora P, Sidarovich A, Krüger N, Kempf A, Nehlmeier I, Graichen L, Moldenhauer AS, Winkler MS, Schulz S, Jäck HM, Stankov MV, Behrens GMN, Pöhlmann S, Hoffmann M. B.1.617.2 enters and fuses lung cells with increased efficiency and evades antibodies induced by infection and vaccination, Cell Reports, 2021, 109825, ISSN 2211-1247, https://doi.org/10.1016/j.celrep.2021.109825
Arora P, Kempf A, Nehlmeier I, Graichen L, Sidarovich A, Winkler MS, Schulz S, Jäck HM, Stankov MV, Behrens GMN, Pöhlmann S, Hoffmann M. Delta variant (B.1.617.2) sublineages do not show increased neutralization resistance. Cell Mol Immunol. 2021 ; https://doi.org/10.1038/s41423-021-00772-y